Certificações e Sistemas de Gestão

Marcação CE e ISO 13485
- Diagnóstico de conformidade (GAP Analysis): (EU) MDR 2017/745 e ISO 13485.
- Planejamento das etapas e definição do caminho regulatório mais apropriado, incluindo a avaliação de conformidade e a seleção do organismo notificado ou certificadora, entre outros.
- Implementação de requisitos para o compliance com o regulamento/norma.
- Suporte técnico em processos de submissão, resposta a não conformidades e auditorias.
- Treinamento para Equipe Técnica e Regulatória.

Auditoria
- Auditoria Mock Up para auditorias ANVISA, VISA e Marcação CE.
- Auditoria Interna.
- Certificações ISO e RDC: Auditorias para certificações específicas como ISO 13485, RDC 665/22.
- Preparação para Certificação CE de acordo com (EU) MDR 2017/745.
Estratégia Regulatória e Clínica

Avaliação Clínica (ANVISA e CE)
- Avaliação da viabilidade de registro por equivalência/comparabilidade.
- Elaboração de Plano de Avaliação Clínica (Marcação CE).
- Elaboração de Plano e Relatório de Revisão Sistemática do produto. equivalente e SOTA.
- Elaboração de Relatório de Avaliação Clínica (ANVISA e Marcação CE)
- Elaboração do Resumo de Segurança e Performance Clínica (SSCP)
- Atualização periódica de documentos existentes (anual ou de acordo com definição da empresa).
- Suporte em resposta aos órgãos reguladores e adequação de documentos já existentes.

Acompanhamento Clínico Pós-Mercado (PMCF)
- Planejamento das atividades de pós-mercado.
- Elaboração do Plano de Acompanhamento Clínico Pós-Mercado.
- Elaboração do Relatório de Acompanhamento Clínico Pós-Mercado.
- Planejamento, acompanhamento e elaboração de relatório de atividades de pós-mercado que não se enquadram em Investigação Clínica.
- Atualização periódica de documentos existentes (anual ou de acordo com definição da empresa).
- Suporte em resposta aos órgãos reguladores e adequação de documentos já existentes.

Investigação Clínica
- Suporte para o planejamento de Investigação Clínica Pré-Mercado, Pós-Mercado ou Benchmarking.
- Elaboração do protocolo do estudo de acordo com a ISO 14155.
- Submissão do protocolo do estudo no comitê de ética em pesquisa em humanos ou ANVISA.
- Elaboração dos documentos essenciais de acordo com a ISO 14155 (Ex. CRF, Brochura do investigador).
- Treinamento da equipe do estudo.
- Monitoramento do estudo.
- Execução da estatística do estudo.
- Elaboração de relatórios parciais ou finais de acordo com a ISO 14155.

Documentação de P&D
- Definição de estratégias de verificação e validação.
- Suporte no planejamento de testes mecânicos, embalagem e reuso.
- Elaboração de protocolos e relatório de testes mecânicos, embalagem e reuso.
- Análise de risco e definição de casos críticos para testes mecânicos, embalagem e reuso.
- Interpretação técnica de resultados de testes mecânicos, embalagem e reuso.
- Adequação documental e suporte em respostas a exigências relacionadas à testes mecânicos.
- Suporte para aplicabilidade das normas ISO 11135, ISO 11137 e ISO 11737 aos processos de esterilização.
Engenharia Aplicada ao Desenvolvimento de Produto

Modelagem 3D
- Criação de modelos 3D para dispositivos médicos.
- Otimização de geometria para prototipagem e fabricação.
- Geração de desenhos técnicos a partir dos modelos 3D.
- Adequação dos modelos às exigências regulatórias.
- Conversão e adaptação entre diferentes plataformas CAD.
- Suporte ao desenvolvimento de produtos em todas as fases.

Protótipos com impressão 3D
- Fabricação de protótipos funcionais e visuais por impressão 3D.
- Validação rápida de conceitos e geometrias.
- Apoio à apresentação de soluções para stakeholders.
- Realização de testes preliminares com agilidade.
- Redução de ciclos de desenvolvimento e retrabalho.
- Suporte à avaliação ergonômica e de montagem.
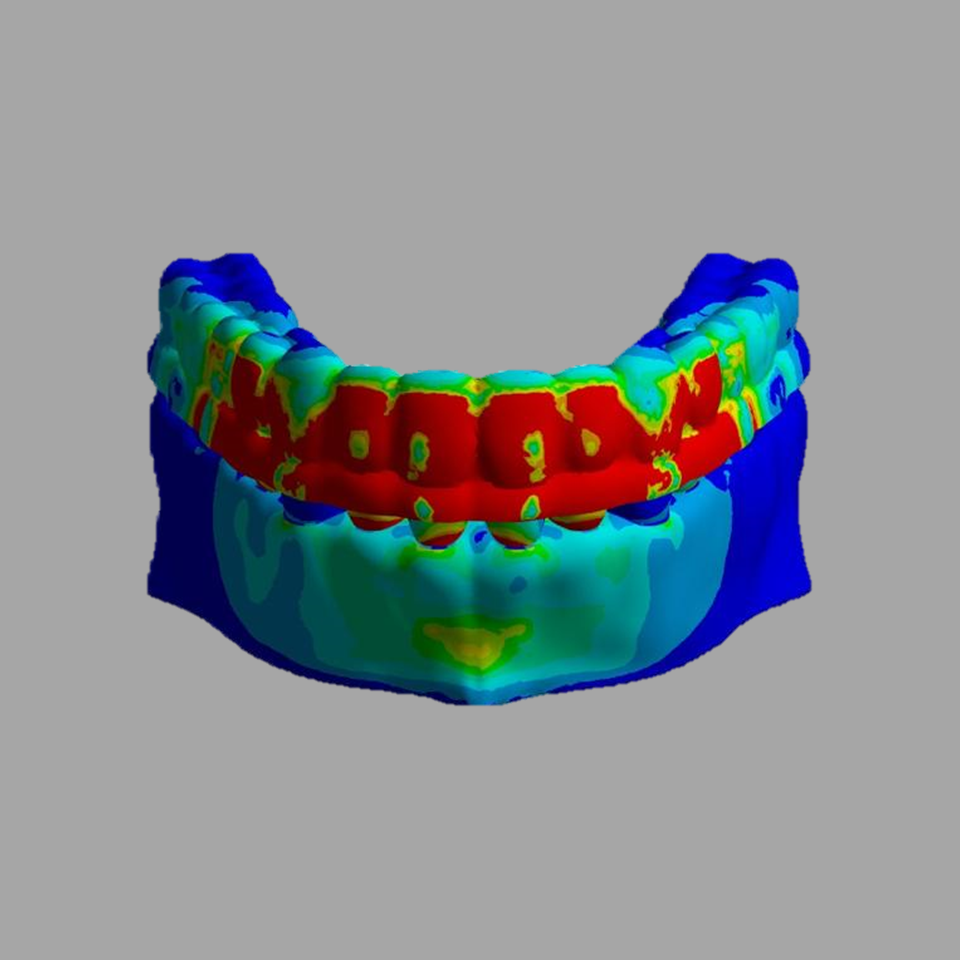
Simulação via Elementos Finitos
- Realização de simulações estruturais por Elementos Finitos (FEA).
- Avaliação de desempenho mecânico de dispositivos médicos.
- Análise de resistência e deformações em condições clínicas.
- Otimização de geometrias e materiais para maior eficiência.
- Suporte à verificação e validação técnica do projeto.
- Geração de relatórios técnicos para submissões regulatórias.
Capacitação Técnica e Regulatória

Treinamentos
- ISO 13485 e RDC 665/22.
- (EU) MDR 2017/745.
- ISO 14155.
- Revisão Sistemática da Literatura.
- Avaliação Clínica.
- Acompanhamento Clínico Pós-Mercado.
- Impressão 3D.
- Desenhos Técnicos.
